Choroby mitochondrialne (zaburzenia mitochondrialne związane z mtDNA) – czym są i jak je diagnozować?
Choroby mitochondrialne (zaburzenia mitochondrialne) są związane z nieprawidłowym działaniem mitochondriów i znajdującym się w nim mtDNA, a czasami również w DNA jądrowym. Jest to spora grupa zaburzeń obejmująca ok. 1500 różnych chorób, a ich częstość występowania szacuje się na 1,5 – 8,5 tysięcy urodzeń [1]. Choroby mitochondrialne należą do grupy wrodzonych chorób metabolicznych. Jakie objawy są najczęściej związane z chorobą mitochondrialną? Jak się diagnozuje choroby mitochondrialne? Czy choroby mitochondrialne są dziedziczne i czy można je leczyć?
Zapraszamy do umówienia się na rozmowę ze specjalistą w sprawie badań genetycznych:
Choroby mitochondrialne – gdzie jest mtDNA?
Choroby mitochondrialne to zaburzenia najczęściej powodowane przez mutacje w mtDNA – DNA mitochondrialnym. Co to oznacza? Przypomnijmy sobie wiedzę z biologii. Każda komórka naszego ciała ma w sobie różne elementy – w tym jądro i mitochondria. Jądro to 'mózg’ komórki – zarządza jej działaniem. Mitochondria z kolei to takie magazyny energii, z których komórka ją czerpie. W jądrze spakowane jest nasze główne DNA – DNA jądrowe, zawierające 23 pary chromosomów i ok. 23 000 genów. Okazuje się jednak, że w mitochondriach również znajduje się DNA – jest ono jednak bardzo krótkie i zawiera 37 geny. Dlatego też w diagnostyce chorób mitochondrialnych bardzo przydatne są badania genetyczne, pozwalające na sprawdzenie źródła problemu – uszkodzone geny. W wielu przypadkach zbadanie samego DNA mitochondrialnego może być niewystarczające, ponieważ DNA jądrowe również może być odpowiedzialne za rozwój chorób mitochondrialnych.
Choroba mitochondrialna – jakie najczęściej daje objawy?

W związku z tym, że mitochondria są odpowiedzialne za magazynowanie energii, zmiany (mutacje) w mtDNA będą wpływać na tkanki i narządy, które najbardziej tej energii potrzebują do prawidłowego działania i tym samym posiadają najwięcej mitochondriów. Narządem, który zużywa najwięcej energii jest mózg i układ nerwowy. U chorego na zaburzenia mitochondrialne może więc dojść do rozwoju takich objawów jak:
- encefalopatia mitochondrialna (MELAS),
- padaczki genetyczne, mioklonie i drgawki,
- opóźnienie rozwoju i objawy autyzmu,
- migreny,
- napady udaropodobne,
- ślepota korowa,
- depresja i zaburzenia lękowe,
- demencja.
Dużej ilości energii zużywają również mięśnie i to układ mięśniowo – kostny oraz serce (które jest mięśniem) jest kolejnym, który jest narażony na zaburzenia w przebiegu chorób mitochondrialnych. Może dojść do rozwoju:
- miopatii (uszkodzenie struktury mięśni, które prowadzi do ich zaniku i osłabienia siły),
- kwasicy (podwyższonego poziomu kwasu mlekowego),
- choroby kardiologiczne,
- nietolerancji wysiłku.

Choroby mitochondrialne mogą również powodować utratę i zaburzenia wzroku (zwyrodnienia siatkówki) i słuchu, zaburzenia ze strony układu pokarmowego, zaburzenia wzrostu i nieprawidłowości endokrynologiczne. Objawy mogą się pojawić w różnym wieku – od dziecięcego po dorosły i u każdego pacjenta choroba może się rozwijać w inny sposób.
Do najczęstszych chorób mitochondrialnych należy zespół Leigha, MELAS, MERRF, choroba Kearnsa-Sayre’a, NARP,
Dziedziczenie mitochondrialne choroby – na czym polega?
Dna mitochondrialne (mtDNA) jest dziedziczone jedynie w linii matczynej – oznacza to, że chorobę mitochondrialną można odziedziczyć tylko po mamie. Nie oznacza to jednak, że mama chorego musi również mieć objawy choroby mitochondrialnej. Może być ona zdrowa i być jedynie nosicielem uszkodzonych genów. ❗ Matka może przekazać mutacje związane z chorobą mitochondrialną zarówno synom jak i córkom. Synowie nie przekażą jej jednak swoim dzieciom. Niestety w przypadku mtDNA nie da się przewidzieć ryzyka zachorowania dziecka.❗
Choroby mitochondrialne – badania mtDNA
W diagnostyce chorób mitochondrialnych wykorzystuje się różne badania, w tym badania genetyczne sprawdzające źródło problemów, czyli mutacje w genach. Przede wszystkim lekarz prowadzący powinien zebrać dokładny wywiad medyczny, dotyczący członków rodziny na tyle pokoleń wstecz ile jest to możliwe. Możliwe jest wykonanie badań biochemicznych z krwi i moczu i oznaczenie konkretnego poziomu danych substancji: stężenie glukozy, kwasu mlekowego, kinazy kreatynowej, ewentualnie karnityny, alaniny, aktywność aminotransferaz [1]. W niektórych przypadkach pomocne może być pobranie płynu mózgowo-rdzeniowego, biopsji mięśni czy rezonansu magnetycznego (MRI). Konieczne mogą się okazać badania okulistyczne i laryngologiczne, a także kardiologiczne.
❗ Zaważyć na diagnozie mogą jednak nowoczesne badania genetyczne dzieci i dorosłych, w tym badanie całoeksomowe WES. Badania takie sprawdzają konkretną przyczynę problemu – konkretne mutacje w mtDNA, ale również w DNA jądrowym.
Badanie mtDNA w badaniu WES
👉 Badanie WES, czyli sekwencjonowanie całego eksomu może być bardzo pomocne (jest ono wykonywane przy pomocy technologii NGS). Dobre badania WES sprawdzają bowiem możliwe przyczyny genetyczne objawów pacjenta – zarówno wszystkie geny w DNA jądrowym jak i DNA mitochondrialnym mtDNA. 👉Przy podejrzeniu choroby mitochondrialnej wykonanie tak szerokiej analizy daje największą szansę na tzw. diagnostykę różnicową – sprawdzenie setek możliwych przyczyn objawów, przede wszystkim wrodzonych chorób metabolicznych.
Oferujemy trzy rodzaje badań WES:
Badanie WES STANDARD, BADANIE WES PREMIUM oraz badanie WES COMPLEX. Jaka jest różnica między tymi badaniami?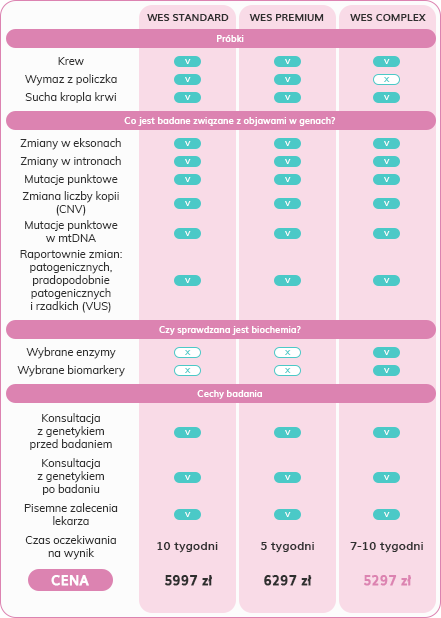
👉 Standardowe badanie WES analizuje najlepiej poznaną część DNA pacjenta, czyli eksony. Poszukuje w nich niebezpiecznych zmian, które będzie można uznać za przyczynę objawów. Badanie WES jest bardzo precyzyjne – każdy gen jest sprawdzany kilkadziesiąt razy, aby mieć pewność co do jego budowy. Dzięki temu wynik jest wartościowy dla lekarza genetyka, który na jego podstawie może podstawić diagnozę danej choroby i zadecydować o dalszym leczeniu.
👉Badania WES PREMIUM oraz WES COMPLEX to badanie WES o rozszerzonym zakresie. Oprócz zmian w eksonach sprawdza dodatkowo zmiany w intronach.
Analiza dotyczy tylko tych zmian w intronach, których działanie jest dobrze poznane, opisane i mogą mieć znaczenie dla diagnozy pacjenta. Pomija się natomiast części intronów, których działania nauka na razie nie potrafi zinterpretować – takie informacje wprowadziłyby jedynie zamieszanie i utrudniły postawienie rozpoznania.
👉Badanie WES COMPLEX to innowacja na rynku badań diagnostycznych. Jest to pierwsze dostępne w Polsce badanie o podejściu tzw. multiomicznym. W trakcie jednej analizy, z jednej pobranej próbki wykonywane jest zarówno bardzo szerokie badanie WES oraz kariotyp molekularny (mikromacierze), a w przypadku wykrycia nieprawidłowości w genach, które mogą odpowiadać za chorobę metaboliczną przeprowadzane jest również badanie biochemiczne. To badanie z kolei umożliwia określenie, czy choroba metaboliczna „jest aktywna” i jak bardzo jest zaawansowana. Widzimy to po poziomie metabolitów we krwi pacjenta.
👉 Bardzo ważnym aspektem podczas wyboru badania WES są certyfikaty, które posiada laboratorium wykonujące analizy. Dlaczego certyfikaty są tak istotne? Ponieważ świadczą o tym, że laboratorium stosuje procedury i wyśrubowane standardy, które zapewniają wiarygodność wyników. Dla pacjenta oznacza to po prostu pewność diagnozy i to, że nic nie zostało przeoczone.
Przeczytaj więcej o istotności certyfikatów oraz na jakie zwrócić uwagę na stronie: https://badamydzieci.pl/porady/certyfikaty-badanie-wes/
UWAGA! mtDNA charakteryzuje się tzw. heteroplazmią. Oznacza to, że w mtDNA pacjenta są zarówno 'zdrowe – prawidłowe’ jak i 'chore – nieprawidłowe’ kopie tych samych mutacji. W niektórych tkankach ilość kopii nieprawidłowych może być mniejsza, w niektórych większa. Diagnoza może więc zależeć od rodzaju pobranej do badania próbki. Czasami konieczne może być więc pobranie dodatkowej próbki i wykonanie dodatkowej ukierunkowanej analizy.
On-line, poprzez sklep: zamów badanie WES
W przypadku badań wymagających pobrania krwi oddzwonimy do Państwa w celu umówienia dogodnego terminu i miejsca pobrania.
Poprzez formularz on-line Rejestracja 24 h/dobę
Oddzwonimy do Państwa w celu potwierdzenia umówienia wizyty.
Telefonicznie: 576 997 525 Rejestracja telefoniczna czynna 7 dni w tygodniu
Pisemnie: biuro@badamydzieci.pl Pisemnie: Facebook MessengerChoroba mitochondrialna – rokowania

Rokowania w przypadku choroby mitochondrialnej są bardzo różne. W zależności od wieku pojawienia się objawów, ale też rodzaju chroby mitochondrialnej będą one inne. Obecnie leczenie chorób mitochondrialnych jest oparte na łagodzeniu objawów. Konieczna jest również minimalizowanie tzw. stresu oksydacyjnego i stosowanie diety i suplementacji witaminowej (np. ryboflawiny – witaminy B2) bogatej w antyutleniacze. W przebiegu chorób metabolicznych podstawą leczenie może się okazać właśnie dieta. Opracowuje się również nowe leczenie farmakologiczne i terapie genowe, które mogą się okazać przełomem i wpłynąć na rokowania pacjenta.
Myślisz o wykonaniu badania WES?
Zachęcamy do bezpłatnej konsultacji:
Najczęściej zadawane pytania
W DOMU:
- Próbkę do badania (krew żylną, suchą kroplę krwi lub wymaz z policzka) może pobrać pielęgniarka mobilna w domu pacjenta.
- Pielęgniarki, które współpracują z nami przestrzegają wszelkich zasad higieny, a zestaw do pobrania próbki jest sterylny i bezpieczny dla pacjenta!
- W przypadku WYMAZU Z POLICZKA oraz SUCHEJ KROPLI KRWI próbką można pobrać samodzielnie, bez pomocy personelu medycznego.
W PLACÓWCE MEDYCZNEJ W CAŁEJ POLSCE
- Współpracujemy z ponad 300 placówkami medycznymi na terenie całek Polski, umówimy Cię na pobranie próbki do badania najbliżej Twojego miejsca zamieszkania.
W Laboratorium testDNA dostępne są następujące badania WES:
- Badanie WES COMPLEX
- Badanie WES PREMIUM
- Badanie WES STANDARD
- Badanie WES PREKONCEPCJA
- Badanie WES PROFILAKTYKA
Dotyczy to zarówno próbki krwi, wymazu z policzka i suchej kropli krwi.
Pobranie krwi jest bezpieczne. Natomiast w niektórych przypadkach w miejscu pobrania krwi (wkłucia) może powstać krwiak, bardzo rzadko może dojść do uszkodzenia nerwów.
Możliwe, że w trakcie pobrania krwi konieczne będzie przytrzymanie dziecka. U dzieci, u których niemożliwe będzie pobranie krwi z żyły odłokciowej, możliwe jest wkłucie się w nietypowe miejsca (u dzieci jest to częsta główka). Może się również zdarzyć, że zajdzie potrzeba kilkukrotnego wkłucia. Jest to standardowa procedura w przypadku pobrań krwi u dzieci i nie należy się tym niepokoić.
Nasze pobrania organizujemy jedynie z personelem medycznym, który ma doświadczenie w pobieraniu krwi u dzieci i noworodków. Osoba pobierająca krew zawsze stara się to zrobić w sposób jak najbardziej komfortowy i przyjazny dla małego pacjenta. Ilość krwi do badania nie jest duża, dlatego najczęściej pobranie przebiega bardzo sprawnie i bezproblemowo.
Terminy oczekiwania na konsultacje z naszymi lekarzami genetykami to od kilku dni do dwóch tygodni (dotyczy to zarówno konsultacji przed badaniem jak i konsultacji wyniku badania).
Termin konsultacji można wybrać samodzielnie korzystając z dostępu do Panelu Klienta.
Istnieje również możliwość płatności odroczonej do 54 dni – PayPo.
Dodatkowo podjęliśmy współpracę z poniższymi Fundacjami. Ich Podopieczni mogą liczyć na zniżki!
„Obywatelska Fundacja Pomocy Dzieciom” https://pomocdzieciom.eu/
POLSKA FUNDACJA POMOCY DZIECIOM NIEDOSŁYSZĄCYM – ECHO http://archiwum.fundacja-echo.pl/
Fundacja “Serca dla Maluszka” https://sercadlamaluszka.pl/
Fundacja „Radość z Uśmiechu” https://radosczusmiechu.pl/
Czas oczekiwania na wynik badania WES PREMIUM to 7 tygodni.
Czas oczekiwania na wynik badania WES COMPLEX to 7-10 tygodni.
- Badanie WES COMPLEX wykonuje się z suchej kropli krwi. Wystarczy, że zamówią Państwo zestaw do pobrania próbek do domu (przesyłamy zestawy również za granicę bez dodatkowych opłat). Natomiast po pobraniu materiału prosimy o jego odesłanie we własnym zakresie do naszego laboratorium.
- Badanie WES PREMIUM można wykonać z suchej kropli krwi. Wystarczy, że zamówią Państwo zestaw do pobrania próbek do domu (przesyłamy zestawy również za granicę bez dodatkowych opłat). Natomiast po pobraniu materiału prosimy o jego odesłanie we własnym zakresie do naszego laboratorium.
- W przypadku pobrania krwi, należy samodzielnie zorganizować takie pobranie w miejscu zamieszkania. Możemy wysłać zestaw do pobrania krwi oraz niezbędną dokumentację na wskazany zagraniczny adres bez dodatkowych opłat. Krew powinna zostać odesłana do Laboratorium w dniu pobrania na koszt pacjenta, dla bezpieczeństwa pobranie powinno się odbyć w poniedziałek lub wtorek.
SUCHA KROPLA KRWI – tak, ponieważ sucha kropla krwi jest idealnym nośnikiem DNA. Próbka może być przechowywana nawet przez kilkanaście dni w temperaturze pokojowej. Jeśli jednak podczas analiz okazałoby się, że materiał DNA nie jest wystarczający aby na jego podstawie wydać wynik, oferujemy Państwu ponowne darmowe pobranie próbki.
Takie sytuacje zdarzają się jednak niezwykle rzadko i są raczej związane z nieprawidłowym pobraniem, aniżeli uszkodzeniem próbki podczas transportu.
WYMAZ Z POLICZKA – tak, ponieważ wymaz z policzka jest bardzo dobrym nośnikiem DNA. Podczas nawet dalekiej podróży (transportem lotniczym) próbka nie traci na jakości. Jeśli jednak podczas analiz okazałoby się, że materiał DNA nie jest wystarczający aby na jego podstawie wydać wynik, oferujemy Państwu ponowne darmowe pobranie próbki.
Takie sytuacje zdarzają się jednak niezwykle rzadko i są raczej związane z nieprawidłowym pobraniem, aniżeli uszkodzeniem próbki podczas transportu.
PRÓBKA KRWI – tak, jeżeli zostanie dostarczona do Laboratorium w przeciągu 72 godzin. Do momentu wysyłki próbki powinna być ona przechowywana w lodówce.
Tak – przed badaniem odbędzie się konsultacja kwalifikująca Pacjenta do badania. Lekarz genetyk nie tylko doradzi czy badanie WES jest odpowiednim rozwiązaniem w danym przypadku, ale również pomoże w wypełnieniu dokumentacji medycznej do badania.
Brak rzetelnej informacji o stanie zdrowia może mieć wpływ na analizę kliniczną i finalny wynik badania. Analiza materiału genetycznego jest indywidualna – ukierunkowana na objawy występujące u Pacjenta i poszukiwanie ich genetycznych możliwych przyczyn, w tym rzadkich zmian w genach (VUS).
Aktualizacja wyniku może być istotna jeżeli u pacjenta pojawiły się nowe objawy kliniczne. Warto również aktualizować badanie WES co kilka lat ze względu na ciągły rozwój medycyny i aktualizację baz danych, do których 'dokładane’ są kolejne istotne dla zdrowia mutacje.
Surowe dane są możliwe do uzyskania na szczególną prośbę pacjenta. W badaniach WES COMPLEX oraz WES PREMIUM są one darmowe. W przypadku badania WES STANDARD dostępne są za dodatkową opłatą.
Surowe dane są przydatne jedynie w momencie kiedy ma się dostęp do analizy bioinformatycznej i stosownego oprogramowania. Lekarz genetyk, a tym bardziej pacjent nie jest w stanie zinterpretować surowych danych samodzielnie.
Jeżeli wykonywana jest od razu analiza TRIO – tak. Materiał DNA rodziców jest porównywany z materiałem dziecka (pacjenta) co daje największe szanse na wykrycie niebezpiecznych mutacji w jednej analizie.
Jeżeli pacjent wykonuje badanie WES pojedyncze, w pierwszym etapie badania WES analizowany jest materiał genetyczny pacjenta. Dopiero na podstawie wyniku badania pacjenta, lekarz genetyk podejmuje decyzję czy rodzina pacjent powinna być również zbadana. Najczęściej taka potrzeba zachodzi w poniższych przypadkach:
- u dziecka wykryto mutację rzadką, o niepotwierdzonej patogeniczności (tzw. VUS). W tej sytuacji rodzice są sprawdzani pod kątem tylko mutacji wykrytej u dziecka. Wynik rodziców ma pomóc w ocenie wpływu mutacji na stan zdrowia pacjenta. Jeżeli rodzice mają tą samą mutację i są zdrowi, można wnioskować, że mutacja ta nie wpływa na stan zdrowia pacjenta. Ocena wyników zawsze należy do lekarza genetyka.
- u dziecka podejrzewa się zmianę, która nie jest dziedziczona (tzw. zmiana de novo). W tej sytuacji jeżeli rodzice nie posiadają danej mutacji, podejrzenie takie jest potwierdzone.
- rodzice chcą wiedzieć jakie jest ryzyko odziedziczenia danej mutacji przez kolejne planowane dzieci i rodzeństwo.
’Bada się wszystkie 23 tys. genów’
To stwierdzenie wymaga sprostowania – aby zrozumieć co jest podstawą analizy KAŻDEGO dostępnego na rynku badania WES i mieć prawidłowe wyobrażenie o tym jak naprawdę przebiega proces badania oraz co jest jej rezultatem – czyli co widnieje na wyniku.
O co więc chodzi z badaniem 'WSZYSTKICH GENÓW’?
Takie stwierdzenie można odnieść do pierwszego etapu analizy – czyli sekwencjonowania. W tym etapie faktycznie wszystkie geny, a właściwie ich części – sekwencje kodujące – są 'rozczytywane’, co oznacza że można poznać ich budowę.
KAŻDE BADANIE WES ZAWIERA TEN PROCES ANALIZY! NIE MOŻNA WIĘC POWIEDZIEĆ, ŻE JEDNO BADANIE WES BADA WSZYTSKIE GENY, A DRUGIE NIE!
Co się dzieje później? Efektem sekwencjonowania są dane bioinformatyczne, które zawierają ogrom informacji (średnio po kilkanaście GIGA dla jednej osoby). Teraz następuje najważniejsza kwestia – czyli odsiew wykrytych mutacji, które mogą być ważne dla Pacjenta i mogą zaważyć na jego diagnozie od tych które nie są istotne.
W tym celu wykonuje się tzw. 'przegląd eksomu’ – jest to pierwszy etap 'odsiewu’. Już na tym etapie można wychwycić mutację, która odpowiada za objawy pacjenta, nie zawsze jednak jest to możliwe.
DLATEGO NAJLEPSZE LABORATORIA NIE POPRZESTAJĄ NA TYM ETAPIE I WYKONUJĄ DODATKOWO TZW. PANELE GENÓW W RAMACH BADANIA WES.
PANELE to zestawy genów, o których wiemy że mogą być powiązane z chorobą występującą u pacjenta (nawet jeśli objawy nie są jednoznacznie ze sobą powiązane). Mogą one zawierać od setek do tysięcy genów.
Wykonując dodatkowo PANELE genów w ramach badania WES bierze się te geny już nie 'pod lupę’, a pod 'mikroskop’ zyskuje się pewność, że żadna, nawet rzadka zmiana nie została przeoczona w trakcie pierwszego etapu 'odsiewu’.
Na wyniku powinny się znaleźć wyselekcjonowanie mutacje – te najważniejsze dla Pacjenta, jeśli oczywiście zostały wykryte.
Podchodząc do badania WES trzeba ZAWSZE pamiętać, że przyczyna choroby niekoniecznie musi być genetyczna, albo może być niemożliwa do wykrycia przy obecnym stanie wiedzy medycznej.
Taka konsultacja może zostać przeprowadzona z rodzicem lub lekarzem prowadzącym (np. pediatrą, neurologiem).
Wynik będzie zinterpretowany przez lekarza genetyka, dzięki czemu pacjent nie będzie miał wątpliwości co do jego znaczenia. Zostanie także poinformowany jak powinno przebiegać dalsze postępowanie.
Dlaczego ‘pusty’ wynik badania to też wartościowy wynik?
Ponieważ oznacza odsianie setek możliwych przyczyn objawów chorego pacjenta.
Dzięki temu można bardzo precyzyjnie pokierować dalszą diagnostyką – to ogromny krok naprzód.
Jeżeli lekarz zobaczy, że został wykonany WES, może automatycznie zrezygnować z podejrzenia wielu chorób wrodzonych. Unikamy zlecania zbędnych badań (również genetycznych – np. pojedynczych genów ‘w ciemno’), czy wizyt u specjalistów. Warto mieć świadomość, że badania pojedynczych genów są również kosztowne (zbadanie jednego genu tą samą metodą, którą wykonywane jest badanie WES to koszt ok. 1000-2000zł), a czas oczekiwania na wynik to kilka tygodni.
Zamiast tego można się skupić na tym co jeszcze możliwe do zrobienia. ‘Czysty’ wynik badania WES może więc oznaczać nie tylko oszczędność finansów i czasu, ale również ograniczenie cierpienia i stresu dziecka związanych ze zbędną diagnostyką.
Zyskujemy też poczucie, że robimy wszystko co się da, aby dotrzeć do przyczyny choroby dziecka.
Są to analizy dostępne w ramach NFZ – lekarze więc rozpoczynając diagnostykę, często w pierwszej kolejności sięgną po te narzędzia.
Co jeżeli badania te nic nie wykazały? Czy oznacza to, że dziecko jest ‘czyste genetycznie’ i przyczyna problemów nie jest związana z genami?
Niestety nie!
KARIOTYP sprawdza budowę dużych elementów DNA – chromosomów. MIKROMACIERZ sprawdza ubytki lub nadwyżki w łańcuchu DNA, natomiast badanie FRAX weryfikuje czy dziecko cierpi na zespół łamliwego chromosomu X.
Wykluczenie tych nieprawidłowości niestety nie oznacza, że przyczyna choroby nie leży w genach! To tylko część diagnostyki, którą można wykonać! Ogromna ilość chorób nie może być wykryta w przy pomocy tych badań.
Dlatego należy drążyć dalej – kolejnym krokiem może być zlecenie badania WES, które jest w stanie zweryfikować tysiące chorób wrodzonych, niemożliwych do sprawdzenia w badaniu KARIOTYPU, MIKROMACIERZY czy FRAX!
Nie, wymienione badania sprawdzają choroby genetyczne na poziomie chromosomów (związane z zaburzeniami liczby lub / i struktury chromosomów), natomiast test WES sprawdza choroby związane z mutacjami punktowymi i zmianami liczby kopii konkretnych genów. Prawidłowy wynik badania NIFTY/SANCO/PAPPA/PANORAMA nie oznacza, że dziecko nie jest obciążone ryzykiem choroby wrodzonej (badania te wykluczają tylko pewien zakres chorób).
Wskazane jest wykonanie obu badań: testu NIFTY w ciąży i testu WES tuż po urodzeniu dziecka. Taki pakiet daje bardzo wcześnie szeroką wiedzę o genetycznym zdrowiu dziecka.
Nie. Wiele chorób genetycznych powstaje 'spontanicznie’ – podczas podziałów komórek zarodka po zapłodnieniu. Na ich powstanie nie można mieć wpływu – jest to sytuacja zupełnie losowa.
Aby zachorować na większość chorób dziedzicznych dziecko musi odziedziczyć 'komplet’ wadliwych genów – od mamy i taty. W przypadku niektórych chorób wystarczy wadliwa kopia genu tylko jednego rodzica. Rodzice jednak nie muszą wiedzieć, że są 'nosicielami’ – mogą być zupełnie zdrowi. Jest to więc również kwestia losowa – nie wolno obwiniać się za chorobę dziecka, na którą nie miało się żadnego wpływu.
W przypadku wykrycia mutacji u dziecka, która może być odpowiedzialna za jego objawy często zleca się badanie rodziców pod kątem tej mutacji. W przypadku badania WES TRIO (włączający do badania rodziców) taka informacja będzie od razu widoczna. Jest ona bardzo istotna z kilku względów. Po pierwsze pomaga ustalić jaki wpływ dana mutacja ma na zdrowie dziecka. Ale również jest ważna jeżeli rodzice planują potomstwo – można świadomie podejść do tej decyzji. Jeżeli w rodzinie jest drugie dziecko to wiedza o dziedziczeniu choroby może pomóc w określeniu ryzyka czy ono również zachoruje. Poznanie takiej informacji to bardzo odpowiedzialne podejście do zdrowia całej rodziny i nie warto się tego obawiać.
NIE MOŻNA SIĘ JEDNAK OBWINIAĆ!
Ważne jest, że w przypadku chorób dziedzicznych żadne z rodziców nie ma wpływu na przekazanie dziecku choroby – jest to sytuacja czysto LOSOWA. Nie można za nią obwiniać ani siebie ani partnera/partnerkę.
Warto jednak jeszcze przed wykonaniem badania porozmawiać na ten temat – co jeżeli jedno z nas lub oboje okażemy się nosicielami wadliwego genu? Jak do tego podejdziemy? Jak zareagujemy? Warto szczerze o tym porozmawiać – również o tym jakie emocje może wywołać taka sytuacja. Pozwolić sobie na ich spokojne przeżycie, w taki sposób, aby nie zaszkodziło to związkowi. Od początku należy mieć świadomość, że NIKT NIE MA NA TO WPŁYWU.
Jeżeli obawiacie się reakcji rodziny/otoczenia można ustalić już przed badaniem, że taka informacja pozostanie między Wami – rodzicami. Nie macie obowiązku dzielić się nią ze światem. Jeżeli jednak postanowicie poinformować o tym rodzinę i boicie się niezrozumienia, ustalcie w jaki sposób ta informacja zostanie przekazana, przygotujcie się na reakcję i odparcie nieprzyjemnych komentarzy.
Nie można więc wykluczyć genetycznego podłoża objawów tylko na podstawie faktu, że do tej pory ta choroba nie objawiała się w rodzinie. Nie wyklucza to też ryzyka, ze wadliwe geny zostaną przekazane kolejnemu pokoleniu.
Badanie WES daje ogromną wiedzę na temat chorób czy też nosicielstwa danej choroby. Test WES jest to badanie bardzo czułe a zarazem bardzo rozległe stąd identyfikuje zmiany, które być może przez całe życie danego człowieka mogłyby nie zostać wykryte. Zdarzają się sytuacje, w których u pacjenta bez żadnych objawów identyfikowane są zmiany, które potencjalnie mogłyby odpowiadać za konkretną chorobę a z różnych przyczyn objawy nie rozwijają się. Stąd specjaliści opisujący wyniki testów WES bardzo ostrożnie podchodzą do interpretacji klinicznej mutacji, biorąc pod uwagę przede wszystkim objawy jakie występują u pacjenta. Ponadto należy również podkreślić fakt, że badania WES mogą wykryć dodatkowo inne zmiany, które nie wynikały z celu badania a mogą mieć znaczenie dla pacjenta. Stąd pacjenci zlecający badania WES powinni zdeklarować czy wyrażają zgodę na raportowanie wszystkich zmian jakie zostaną zidentyfikowane w badaniu WES. Badanie WES nie wykryje również tzw. mutacji dynamicznych. Niekiedy wynik badania WES należy potwierdzić inną metodą (np. Sangera lub MLPA). Ewentualne wskazanie do wykonania dodatkowych badań zawsze daje lekarz genetyk interpretujący wynik.
Istnieją spore różnice pomiędzy wynikami badania WES lub innych badań NGS (np. panelowych) wykonywanych w różnych laboratoriach. Mogą one dotyczyć klasyfikacji do raportowania mutacji rzadkich o nieokreślonej patogeniczności, mutacji łagodnych i potencjalnie łagodnych. Tego typu zmiany z dużym prawdopodobieństwem nie stanowią ryzyka rozwoju objawów choroby, w związku z tym mogą nie zostać zaraportowane. Decyzję taką podejmuje diagnosta laboratoryjny (który bierze odpowiedzialność za finalny wynik) na etapie analizy klinicznej eksomu Pacjenta. W klasyfikacji do raportowania uznaje się kilka czynników: częstość występowania zmiany w populacji zdrowej/chorej, określenie zmiany w wybranych bazach danych jako łagodna/potencjalnie łagodna, informacje z literatury specjalistycznej, objawy kliniczne Pacjenta. Dostęp do tego typu informacji przez poszczególne laboratoria może się różnić! Na ten moment nie istnieje standard dotyczący raportowania tego typu zmian.
Wybierają badanie WES zwróć więc uwagę przede wszystkim na to:
- czy badanie jest poprzedzone konsultacją genetyczną – co ma wpływ na WYBÓR GENÓW DO ANALIZY
- z jakich baz danych korzysta laboratorium – najlepsze badania WES wykorzystują PŁATNE bazy danych
- jaka jest wysokość pokrycia genów – powinna być ona minimum x100
- czy laboratorium jest certyfikowane – np. przez Europejską Agencję Kontroli Badań Genetycznych, co jest gwarancją spełnienia wyśrubowanych norm jakościowych
- jaki jest ZAKRES analizy – co ma wpływ na to ile chorób i zaburzeń zostanie sprawdzonych. Najszerszym badaniem WES w Europie jest WES COMPLEX, sprawdza ono EKSONY + INTRONY + mtDNA + zmiany CNV+ badanie metaboliczne, sprawdzające wybrane enzymy i biomarkery
Na wyniku badania WES zaraportowane mutacje zawsze zostaną opatrzone opisem/informacją do jakiego wariantu patogeniczności zostały zakwalifikowane. Jak można zakwalifikować wykryte u pacjenta warianty?
Wariant patogenny: wykryty wariant może zostać uznany za bezpośrednią przyczynę choroby. Należy jednak pamiętać, że istnieje wiele zaburzeń, które są spowodowane mutacjami w kilku genach, jeden patogeniczny wariant może więc mieć tzw. 'niepełną penetrację’.
Wariant prawdopodobnie/potencjalnie patogenny: wykryta zmiana z dużym prawdopodobieństwem może zostać uznana za przyczynę choroby. Natomiast nie można mieć takiej pewności (dane naukowe na to nie pozwalają).
Wariant o nieokreślnej/nieznanej patogeniczności: wykryta zmiana może być powiązana z objawami pacjenta, ale nie można jednoznacznie określić jej znaczenia. Tego typu wariantów nie powinno się raportować na wyniku jeśli nie są one związane z objawami pacjenta (czyli na wyniku badań wykonywanych na przykład w celach profilaktycznych).
Wariant prawdopodobnie łagodny/łagodny: prawdopodobnie wykryta mutacja nie ma żadnego związku z występowaniem objawów choroby u pacjenta (tego typu zmiany nie zostaną zaraportowane na wyniku badania WES).
Jak kwalifikuje się wykryte u pacjenta warianty do poszczególnych grup? Służą do tego wytyczne American College of Medical Genetics and Genomics i American Association for Molecular Pathology (S. Richards, Genet Med. 2015 May;17(5):405-24).
Wytyczne te biorą pod uwagę na przykład:
- występowanie danej mutacji w bazach danych
- potwierdzone przypadki kliniczne pacjentów na świecie
- częstość występowania danej mutacji w populacji. Przyjmuje się, że jeżeli dany wariant występuje >5% w danej populacji to jest określany jako łagodny
Źródła:
[1] Choroby mitochondrialne – diagnostyka i postępowanie, dr n. med. Hanna Mierzewska, Klinika Neurologii Dzieci i Młodzieży, Instytut Matki i Dziecka, Warszawa, 2017, Neurologia po dyplomie